El uso de la ingeniería genética en el diseño y mejoramiento de la microbiota intestinal
Fernanda Cornejo-Granados y Adrián Ochoa-Leyva
En 1887, Robert Koch demostró que el agente causante del ántrax era una bacteria [1], y pasaron 100 años para descubrir que esa bacteria tenía dos fragmentos de ADN adicionales a su genoma que contenían los genes responsables de la enfermedad. Posteriormente, en 1952, J. Lederberg propuso el término “plásmido” para designar a estos fragmentos de ADN capaces de reproducirse de forma autónoma [2]. Por supuesto, estos fueron tiempos extraordinarios para la genética molecular. J. Watson y F. Crick propusieron la estructura de la doble hélice del ADN (1953) [3;4]. A. Kornberg describió cómo se lleva a cabo la síntesis del ADN (1958), aislando por primera vez a la proteína responsable de sintetizar una nueva cadena de ADN, a partir de una ya existente: la ADN polimerasa, y logrando crear artificialmente una cadena de ADN sin la ayuda de una célula [5]. Estos descubrimientos establecieron las bases de la ingeniería genética, ampliamente utilizada en nuestros días.
Sin embargo, nos tomó 20 años entender mucho de la biología de los plásmidos: ¿cómo se autocopian?, ¿cómo se mueven?, ¿cómo adquieren y transmiten genes?, y ¿cómo se comunican entre ellos y con la célula que los hospeda? Ello permitió que, en la década de 1970 se comenzaran a utilizar masivamente como vectores (vehículos) acarreadores de genes. Es decir, se descubrió que podíamos insertar un gen (clonar) con una función específica (degradar el almidón), a una molécula de ADN (plásmido) y al insertar dicha molécula en una bacteria (transformar) le otorgaba la capacidad de degradar el almidón. Una de dichas moléculas fue el plásmido pBR322, creado en el laboratorio del Dr. Herbert Boyer en la Universidad de California, San Francisco, por los investigadores postdoctorales Francisco Bolívar Zapata (hoy Investigador Emérito en nuestro Instituto) y Raymond L. Rodríguez (de ahí la “B” de “Bolívar” y la “R” de “Rodríguez” en el pBR322). En aquellos tiempos se demostraría también que genes de células animales pueden introducirse en bacterias, mediante un plásmido.
Los plásmidos, una herramienta para mejorar la microbiota
Los plásmidos pueden llevar consigo genes de resistencia a antibióticos, virulencia, toxinas, genes de resistencia y degradación de agentes tóxicos, entre otros, los cuales dan ventajas a las bacterias que los hospedan, ofreciéndoles propiedades con potencial aplicación médica, agrícola y ambiental. Esta capacidad de acarrear funciones “a la medida”, abre las puertas para utilizar a los plásmidos como vehículos para cambiar las propiedades de comunidades microbianas, como la microbiota. Siendo esta la comunidad de bacterias que habita naturalmente dentro de humanos y animales (ver BiotecMov No. 5:2), manteniendo una íntima relación con quien la hospeda, ayudando a mantener la salud.
Las tecnologías de secuenciación masiva (ver BiotecMov No. 13 ). desarrolladas en la década de los 2000, nos permiten conocer la secuencia de cualquier hebra de ADN y con ello identificar los genes o microorganismos que se encuentran presentes en cualquier muestra, por ejemplo, saliva, agua, suelo, comida, entre otros [6]. Actualmente, gracias a la creación de secuenciadores de ADN de mayor capacidad, podemos conocer la secuencia de miles de hebras de ADN simultáneamente, lo que nos permite identificar a todas las bacterias presentes en comunidades complejas (como la microbiota), sin necesidad de cultivarla y, por otra parte, identificar cómo esta comunidad se altera cuando surge una enfermedad.
Por otro lado, ya que conocemos a las bacterias importantes para un ambiente, gracias a la tecnología del ADN recombinante podemos introducir genes en ellas para llevar funciones que permitan regresar a la comunidad al estado sano. A este proceso le llamamos “ingeniería de la microbiota” (Figura 1).

Figura 1. Gracias al desarrollo de las ciencias ómicas conocemos las alteraciones que sufre la microbiota cuando hay una enfermedad. Hoy ese conocimiento nos permite aplicar la ingeniería genética para revertir la microbiota a un estado sano. Creado con BioRender.com
Pasos para la ingeniería de la microbiota
La ingeniería de la microbiota se puede llevar a cabo mediante la introducción de plásmidos o modificando el genoma bacteriano. Estos cambios pueden generar funciones beneficiosas para el hospedero, sin necesariamente cambiar al resto de la comunidad bacteriana. O bien, pueden generar cambios en la comunidad bacteriana y esto a su vez tener un efecto positivo en el hospedero (Figura 2). Dicho proceso implica cuatro pasos generales: 1) aislar la bacteria que llevará las funciones nuevas. Idealmente, esta debe ser un residente natural de la microbiota para facilitar que, cuando sea modificada, pueda regresar a colonizar el nicho que ya conocía y volver a comunicarse con las demás bacterias; 2) editar el ADN (plásmido o genoma) para que produzca las funciones que nos interesa ingresar a la comunidad; 3) introducir el ADN modificado a la bacteria, atravesando su membrana, y 4) caracterizar la microbiota del nicho al que ingresamos nuestra bacteria, para conocer los cambios que ocurrieron al introducir funciones nuevas [7] (Figura 2A).
Aplicaciones de la ingeniería de la microbiota
Gracias a estas herramientas, podemos adecuar y programar a las bacterias de la microbiota para que perciban y respondan a lo que pasa a su alrededor, generando beneficios al hospedero.
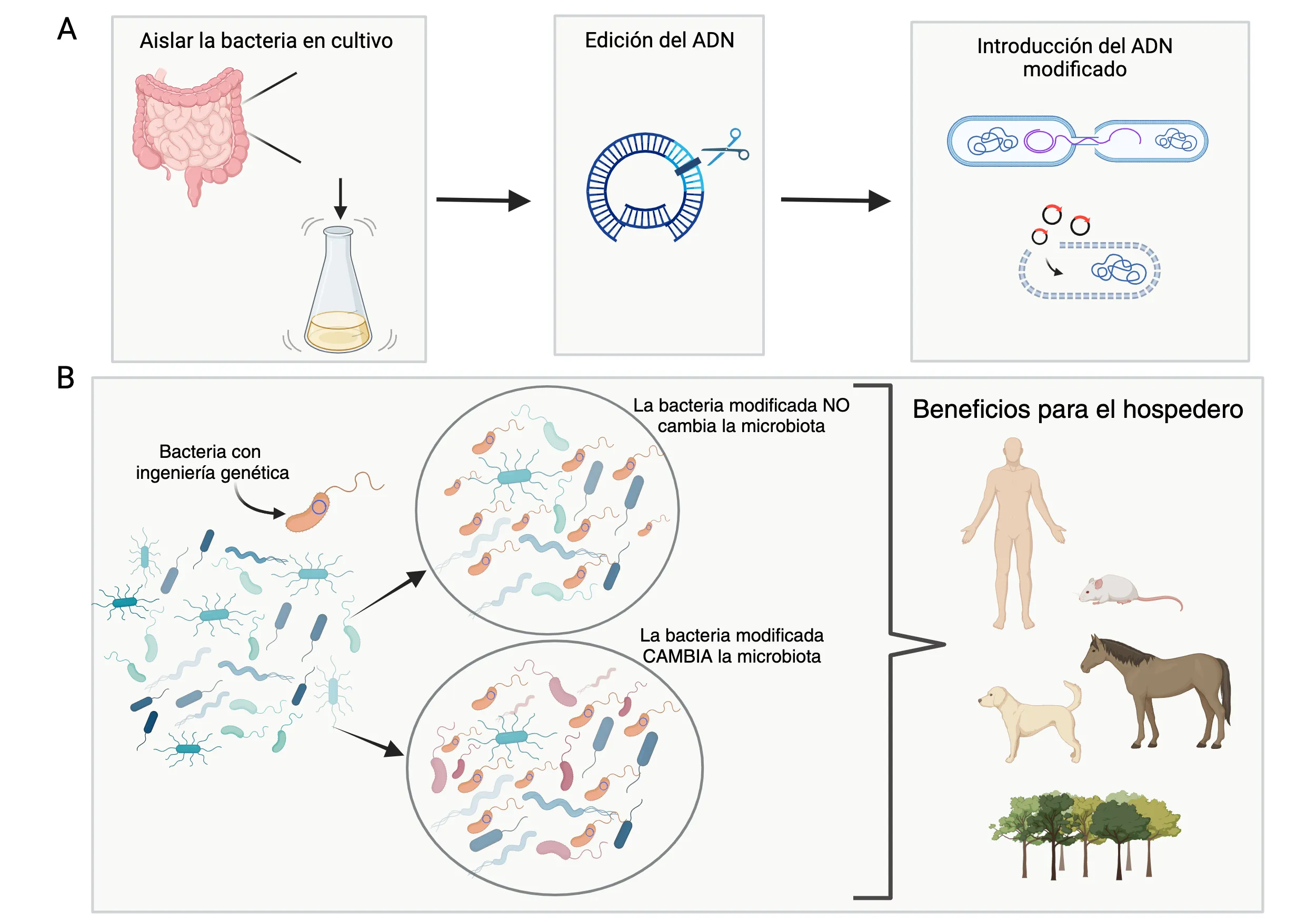
Figura 2. A) La ingeniería de la microbiota implica aislar la bacteria que llevará el ADN modificado, la edición del ADN, la introducción del ADN modificado a la bacteria aislada y B) introducir la bacteria modificada en la microbiota donde lleva a cabo las funciones nuevas y producen beneficios en el hospedero. Creado con BioRender.com
Existen diversos ejemplos de cómo esta tecnología ha logrado aplicarse para mejorar la salud de humanos y animales. En un estudio, se modificó el ADN de la bacteria L. lactis, dándole la capacidad de producir tagatosa: una proteína capaz de degradar moléculas de azúcar. Posteriormente, cuando la bacteria con ADN modificado se administró oralmente a ratones, se observó que, gracias a la tagatosa, los niveles de glucosa en la sangre de los ratones disminuían. Asimismo, otro estudio clínico demostró la mejora de pacientes intolerantes a la lactosa (un tipo de azúcar que se encuentra naturalmente en la leche), después de consumir a la bacteria L. reuteri, la cual, gracias a la ingeniería genética, tenía la capacidad de producir lactasa, la proteína capaz de romper las moléculas de lactosa, y con ello mejorar los síntomas de la intolerancia a productos con leche.
Otras bacterias se han adecuado para fortalecer el sistema inmune. Por ejemplo, la bacteria L. lactis fue modificada al introducirle una molécula de ADN que le dio la capacidad para producir interleucina 27, la cual es una molécula que ayuda a nuestro sistema inmune a disminuir la inflamación. Después de que esta bacteria modificada fue administrada oralmente a ratones, se demostró que puede ayudar en el tratamiento del síndrome de intestino irritable, el cual se caracteriza por una inflamación excesiva del intestino grueso [8].
Por otro lado, muchas bacterias producen naturalmente moléculas, llamadas bacteriocinas, las cuales,
al ser liberadas al medio, inhiben el crecimiento de otras bacterias que buscan establecerse y compiten
por los nutrientes disponibles. En un trabajo de investigación, aprovecharon este mecanismo y
modificaron a la bacteria Lactobacillus reuteri para que produjera tres veces más la
De manera natural, las bacterias pueden percibir la presencia de nutrientes, los niveles de ácido o la presencia de otras bacterias a su alrededor. En este sentido, en otro trabajo de investigación, modificaron a la bacteria E. coli, introduciendo un gen que le dio la capacidad de percibir proteínas propias de tumores en el hígado. Una vez que la bacteria fue administrada a ratones, ésta fue capaz de detectar las proteínas tumorales y responder produciendo otra proteína (que es fluorescente) y que puede ser detectada con equipos especializados. Así, la ingeniería genética aprovecha las capacidades naturales de la bacteria en favor de la salud de humanos y otros animales [8].
El conocimiento y la caracterización de las comunidades microbianas y en especial de la microbiota, nos ha revelado la profunda contribución que tienen en nuestra vida. Hoy, aquellos descubrimientos iniciales sobre el ADN recombinante y los resultados derivados de la secuenciación masiva nos abren una oportunidad sin precedentes para diseñar estrategias terapéuticas o de prevención, que mejoren nuestra vida, basadas en la ingeniería de nuestra microbiota. En este sentido, genetistas, biólogos, químicos, biólogos computacionales, profesionales de la salud, entre otros, nos enfrentamos a retos para lograr que esta tecnología avance en favor del cuidado de la salud de humanos y animales.
Referencias
- Koch R. (1877). The etiology of anthrax, based on the life history of Bacillus anthracis. Beitriige Znr Biologic Dee Pflanzen 2:277–310.
- Lederberg J. (1952). Cell genetics and hereditary symbiosis. Physiol Rev 32:403–430.
- Crick FHC, Watson JD. (1953). Molecular structure of nucleic acids: a structure for deoxyribose nucleic acid. Nature 171:737–738. DOI: 10.1152/physrev.1952.32.4.403
- Zurita M. (2023). 70 años de la doble hélice. Biotecnología en Movimiento 33-1:1-7.
- Kornberg A. (1960). Biologic synthesis of deoxyribonucleic acid. Science 131:1503–1508. DOI: 10.1126/science.131.3412.1503.
- Grande Cano R (2018) Secuenciación Masiva de ADN. Biotecnología en Movimiento. 133-4: 13-21
- Lawson C, et al. (2019). Common principles and best practices for engineering microbiomes. Nat Rev Microbiol 17, 725-741. DOI: 10.1038/s41579-019-0255-9
- Inda ME, et al. (2019) Emerging frontiers in microbiome engineering . Trends in Immunology 40, 952-973. DOI: doi.org/10.1016/j.it.2019.08.007.
Comparte este artículo en redes sociales

Acerca de los autores
Los autores forman parte del Departamento de Microbiología Molecular del IBt. La Dra. Fernanda Cornejo-Granados es investigadora posdoctoral del programa Estancias Posdoctorales por México 2022 de CONAHCyT y el Dr. Adrián Ochoa-Leyva es Investigador Titular y Líder Académico.
Contacto: adrian.ochoa@ibt.unam.mx